神经纤维瘤
Neurofibroma
同义词(或曾用名): 局限性神经纤维瘤、弥漫性神经纤维瘤、上皮样经纤维瘤、色素性神经纤维瘤、非典型性神经纤维瘤、软组织巨神
概述:
神经纤维瘤是良性周围神经鞘膜肿瘤,由施万细胞、纤维细胞母及少量的轴突、神经束膜细胞共同构成。
发病部位: 任何年龄均可受累,但最常见于年轻成人。
诊断要点:
任何年龄均可受累,但最常见于年轻成人;
通常发生于全身的皮肤或皮下组织;大体表现为界清楚的纺锤形病变,常与神经干有关;切面质硬、灰白色;
丛状病变是一种多结节成簇的病变,好像一袋“蠕虫”;
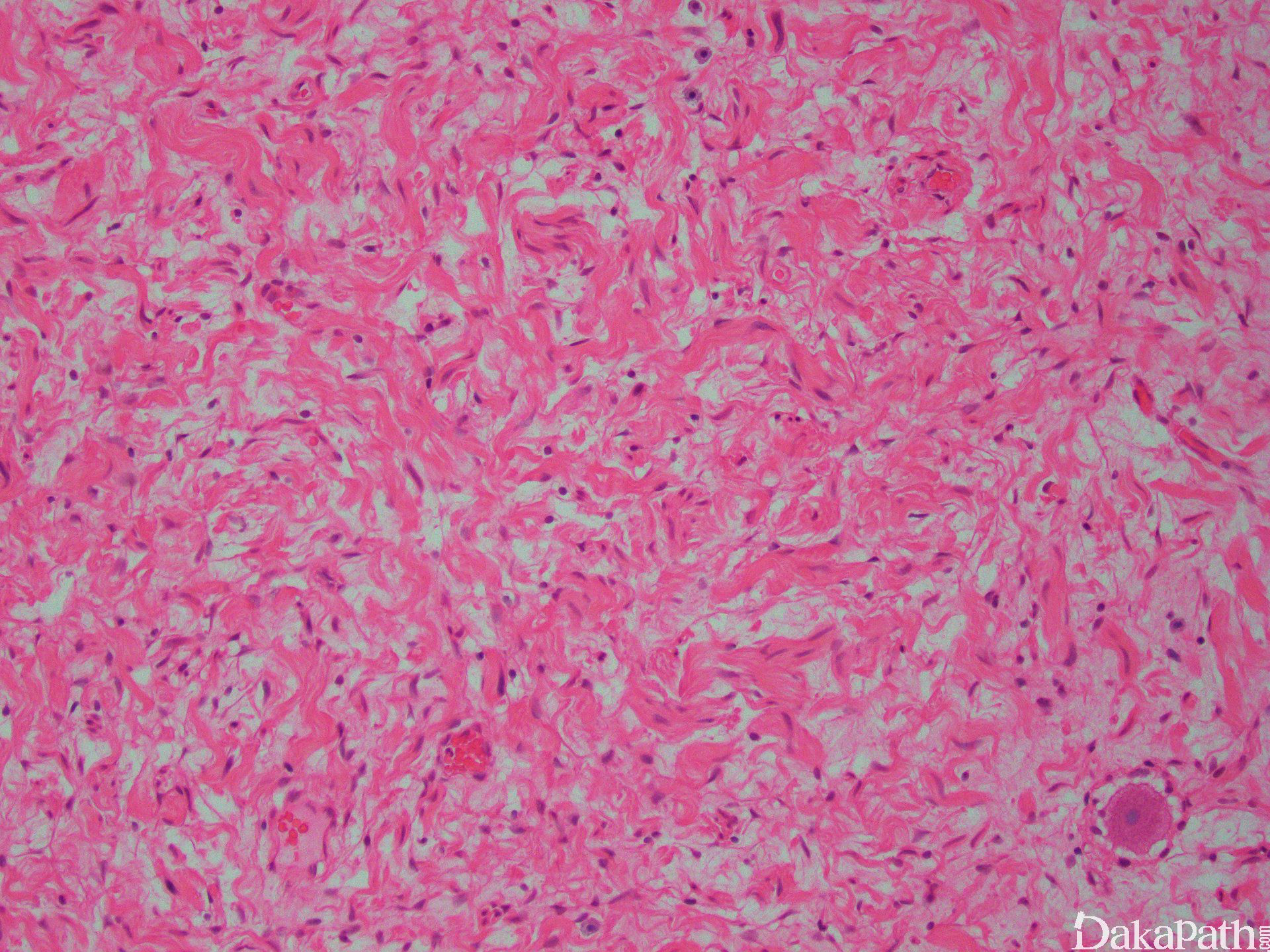
低至中度富于细胞的病变,由具有波纹状细胞核和嗜酸性胞质的细胞组成,散在有胶原纤维束;
间质可出现少量黏液性物质或呈黏液样改变,偶见玻璃样变;
常见轻度核的非典型性,但不代表是恶性变;
根据临床及形态特点不同,可分为局限性神经纤维瘤、丛状神经纤维瘤、弥漫性神经纤维瘤、上皮样经纤维瘤、色素性神经纤维瘤、非典型性神经纤维瘤、软组织巨神经纤维瘤、伴有假菊形团的树突状细胞神经纤维瘤等。
局限性神经纤维瘤:
施万细胞是最主要的成分,为纤长的梭形细胞,其核纤长尖细,可呈波浪形,染色质深染,胞质淡伊红色或透亮;
瘤细胞往往呈束状,平行波浪排列,间质多为疏松水肿样,浅蓝色;
丛状神经纤维瘤:
几乎总是伴有 NF1;
不规则膨大的神经束显示多结节性外观;
细胞通常稀疏,伴有显著的黏液样基质;
可见不同程度的核的多形性;
核分裂活性少见;
弥漫性神经纤维瘤:
肿瘤细胞伸展到皮肤和皮下组织,并包绕皮肤附属器结构;
间质多为均质纤细的胶原,施万细胞散布间质中,细胞呈短梭形或圆形;
瘤内可见成簇状分布的触觉小体;
上皮样经纤维瘤:部分瘤细胞呈上皮样,细胞核大,胞质丰富,淡红染,核呈圆形、卵圆形或多边形;间质似淀粉样变或玻璃样变;
色素性神经纤维瘤:含有多少不定的含黑色素颗粒的瘤细胞,色素细胞呈树突状或上皮样。
非典型性神经纤维瘤:细胞密度明显增加,伴有或不伴有核分裂象;
软组织巨神经纤维瘤;
最少见,仅发生于 I 型神经纤维瘤的患者;
患者皮肤色素沉着,局部和弥漫的肥厚、松垂,若发生在下肢,形成神经瘤性象皮肿;
伴有假菊形团的树突状细胞神经纤维瘤:
常表现为皮肤表面孤立边界清楚的结节性肿块;
肿物由两种细胞成分构成:一种细胞体积较小,深染,胞质较少,似淋巴细胞样,称为 I 型细胞;另一种细胞体积较大,核呈空泡状,淡染,可见核沟和核内包涵体,胞质丰富淡染,称为 II 型细胞;
I 型细胞呈同心圆状围绕在 II 型细胞周围,形成假菊形团;细胞异型性不明显,核分裂象不易见到。



免疫组织化学染色:
S-100. MBP、XIIIa、CD34 阳性,可见 EMA 阳性神经束膜细胞,NF 阳性的轴突成分。
鉴别诊断:
神经鞘瘤 :有 Antoni A 和 Antoni B 结构,常出血、囊性变;
真皮纤维瘤 :瘤细胞形成漩涡或车辐状结构,漩涡中心有组织细胞;
隆突性皮肤纤维肉瘤 :属中间型成纤维母细胞性肿瘤,瘤细胞具轻度异型性,核分裂象易见,瘤细胞呈 CD34(+),S100(-)。
预后:
局部切除多可治愈,极少数局限性神经纤维瘤可发生恶变。
治疗:
局部完整切除。
参考文献:
Thareja S et al: Glomus-like bodies within a neurofibroma: a novel neoplasm arising in neurofibromatosis type 1 or a coincidence? J Cutan Pathol. 42(4):285-8, 2015
Harder A et al: Hybrid neurofibroma/schwannoma is overrepresented among schwannomatosis and neurofibromatosis patients. Am J Surg Pathol. 36(5):702-9, 2012
Shaw CM et al: Elevated expression of IRS2 in the progression from neurofibroma to malignant peripheral nerve sheath tumor. Anticancer Res. 32(2):439-43, 2012
Yeh I et al: Distinguishing neurofibroma from desmoplastic melanoma: the value of the CD34 fingerprint. J Cutan Pathol. 38(8):625-30, 2011
Gesundheit B et al: The role of angiogenesis in the transformation of plexiform neurofibroma into malignant peripheral nerve sheath tumors in children with neurofibromatosis type 1. J Pediatr Hematol Oncol. 32(7):548-53, 2010
Jokinen CH et al: Atypical neurofibroma of the skin and subcutaneous tissue: clinicopathologic analysis of 11 cases. J Cutan Pathol. 37(1):35-42, 2010
Magro G et al: Multinucleated floret-like giant cells in sporadic and NF1-associated neurofibromas: a clinicopathologic study of 94 cases. Virchows Arch. 456(1):71-6, 2010
Spurlock G et al: Molecular evolution of a neurofibroma to malignant peripheral nerve sheath tumor (MPNST) in an NF1 patient: correlation between histopathological, clinical and molecular findings. J Cancer Res Clin Oncol. 136(12):1869-80, 2010
Gregorian C et al: PTEN dosage is essential for neurofibroma development and malignant transformation. Proc Natl Acad Sci U S A. 106(46):19479-84, 2009
Motoi T et al: Pigmented neurofibroma: review of Japanese patients with an analysis of melanogenesis demonstrating coexpression of c-met protooncogene and microphthalmia-associated transcription factor. Hum Pathol. 36(8):871-7, 2005
Val-Bernal JF et al: Cutaneous lipomatous neurofibroma: characterization and frequency. J Cutan Pathol. 32(4):274-9, 2005
Skovronsky DM et al: Pathologic classification of peripheral nerve tumors. Neurosurg Clin N Am. 15(2):157-66, 2004
← 神经鞘瘤 色素性恶性周围神经鞘瘤 →
